Как работает генная терапия
Генная терапия — общее название технологий (а также соответствующих лекарственных средств), направленных на внесение изменений в генетический аппарат соматических клеток человека для лечения различных заболеваний. Гены закодированы в дезоксирибонуклеиновой кислоте (ДНК) и содержат всю информацию, необходимую для формирования и жизнедеятельности клеток. История развития генной терапии началась в 1972 году, когда американские ученые из Стэндфордского университета обнаружили явление прямого переноса фрагментов ДНК от одной бактерии кишечной палочки к другой при непосредственном контакте этих клеток.
Незначительные изменения в ДНК генов — так называемые генетические вариации — могут провоцировать развитие серьезных заболеваний. Такие изменения возникают при неправильном копировании информации, закодированной в генах: это приводит к образованию неполноценных белков, которые и вызывают болезни. Генная терапия используется для устранения первопричины недуга, что позволяет тканям и органам начать функционировать нормально. Простыми словами, метод ориентирован на исправление дефектов, вызванных изменениями в структуре ДНК, например, в результате поражения вирусом.
Показания для применения генной терапии
Генная терапия рассматривается как потенциально универсальный подход к лечению широкого спектра недугов. Это могут быть наследственные, мультифакториальные и инфекционные заболевания, злокачественные образования и пр. Среди заболеваний, для которых разрабатываются методы генной терапии, значительная часть приходится на различные виды рака. Злокачественная трансформация клетки происходит в результате накопления генетических дефектов, приводящих к аномальному росту. Непосредственной причиной является дисбаланс в пролиферации и гибели клеток. Поэтому разработка способов коррекции этих дефектов является основой генной терапии злокачественных новообразований.
| | Одна из новейших технологий в генотерапии рака — это технология "молчащих генов". В данном типе генотерапии используется явление так называемой РНК-интерференции или РНК-сайленсинг. Пациенту вводится определённый коктейль малых интерферирующих РНК, которые заставляют замолчать те гены, которые активно работают в опухоли. Это вызывает либо нокаут этих генов, либо выраженное снижение их экспрессии, например, протоонкогенов или генов роста или полиферации любой ткани. Таким образом, происходит генетическое подавление опухолевой прогрессии, — рассказала Zdrav.Expert врач-генетик крупной медицинской компании, доктор медицинских наук Лиля Джемилева. | |
Технологии генной терапии
Типы генов, используемых при соответствующей терапии, разнообразны, а их выбор определяется механизмами развития заболевания. Одной из сложнейших проблем в генной терапии является доставка требуемого гена в нужные ткани при минимизации его контакта с биологическими средами организма до достижения клетки-мишени, а также обеспечение доставки гена в нужную клетку с целью его эффективной и безопасной работы в ней.
Трансфекция вируса
В данном случае полноценная ДНК вносится в вирус посредством химической реакции, а затем этим вирусом заражают (трансфицируют) клетки человека, что приводит к перемещению ДНК в ядра этих клеток. Однако при данном подходе может наблюдаться серьезный побочный эффект: существует риск реакции организма на вирус, аналогичной реакции на инфекцию.
| | Основным путём доставки в клетку нужного генетического материала является вирусный вектор. Для этого чаще всего используются аденовирусы, поскольку они широко распространены в человеческой популяции в виде аденовирусной инфекции, которую каждый из нас может переносить в детстве. В этот видоизменённый вирус, у которого удалена вирусная ДНК, но сохранена вирусная оболочка, внедряют копию нужного гена. Такой вариант терапевтического материала часто используют для генотерапии заболеваний, — отмечает Джемилева. | |
Липосомы
Данный метод генной вставки базируется на применении липосом — сферических везикул, имеющих один или несколько липидных бислоев. Они поглощаются клетками, что позволяет доставлять ДНК в определенные части организма.В «Т1» — большое укрупнение. TAdviser составил карту активов холдинга 
Использованием антисмысловых нуклеиновых кислот
Данный метод нацелен на отключение функций патологических генов. Специальные лекарственные препараты соединяются с определенными фрагментами ДНК, предотвращая функционирование затронутых генов. Способ нацелен прежде всего на терапию злокачественных образований. Тем не менее, эта методика обладает потенциалом большей эффективности и безопасности в сравнении с терапией генной вставкой.
Трансплантационная терапия
При этом подходе производится изменении генов в пересаженных органах. Это снижает вероятность отторжения у реципиента, что повышает шансы на успех хирургической операции. В результате, получателю трансплантата может не требоваться прием специальных препаратов, подавляющих иммунную систему.
Химическая модификация
Суть метода заключается в повышении или снижении активности определенных генов посредством изменения клеточных химических реакций, контролирующих экспрессию генов. Благодаря этому способу можно, например, контролировать выработку определенных белков. Метод подходит для лечения некоторых видов злокачественных образований.
CRISPR/Cas9
Основная статья: CRISPR (система редактирования генов)
Это мощные инструменты генной модификации, которые открывают новые возможности в плане устранения причин наследственных заболеваний и повышения устойчивости организма к старческим недугам. Нужный эффект достигается путем коррекции исходной ДНК либо встраивания нового гена в конкретное место ДНК.
Препараты генной терапии
Основная статья: Генотерапевтические препараты
К августу 2023 года разработаны биологические лекарственные препараты, в которых активное вещество содержит или состоит из рекомбинантной нуклеиновой кислоты, используемой для регулирования, замены, добавления или удаления генетической последовательности. В качестве примера можно привести препарат «Золгенсма», который применяется для лечения спинальной мышечной атрофии (СМА) у детей до двух лет. Однако стоят такие лекарства крайне дорого: цена дозы (вводится однократно) превышает $2 млн.
| | Как и любая терапия или лекарственные препараты, генотерапия также имеет побочные эффекты, опасности и противопоказания. Первое — это опасность доставки генетического материала не в тот тип клеток и, соответственно, неэффективность введения того или иного генотерапевтического препарата. Второе — если эти препараты каким-то образом модицифированы и конкретно вносят изменения в геном пациента, то это чревато возникновением различных клонов злокачественных клеток из-за видоизменения генетического материала пациента. Третье — риск манифестации вирусных инфекций при использовании различных вирусных конструкций, — говорит Джемилева. | |
Хроника
2025
Прорыв в генной терапии: ИИ превзошел эволюцию в синтезе важнейших элементов ДНК
В ходе транснационального исследования в области генетики были созданы синтетические регуляторные элементы ДНК с помощью генеративного искусственного интеллекта. Результаты работы опубликованы в журнале Nature Genetics 23 декабря 2025 года.
Группа ученых (под руководством специалистов онкоцентра Массачусетской больницы общего профиля Лукаса Феррейра ДаСилвы и Саймона Сенана) разработала алгоритм DNA-Diffusion для проектирования регуляторных участков ДНК — фрагментов, отвечающих за экспрессию генов.
Алгоритм представляет собой систему на основе ИИ, которая обучается на данных об активности ДНК в разных типах клеток и создает короткие регуляторные последовательности, работающие только в определенных клетках.
DNA-Diffusion генерирует синтетические элементы длиной 200 пар оснований. Эти последовательности повторяют принципы, по которым к ДНК присоединяются природные регуляторные белки, но при этом демонстрируют более высокую специфичность к целевым типам клеток. Работу элементов проверили с помощью библиотеки из 5 850 последовательностей (методом STARR-seq) в трех линиях клеток.
Ключевым результатом стала успешная активация природного гена AXIN2 в его естественном положении в геноме (с использованием метода EXTRA-seq). Этот ген обладает защитными свойствами против лейкемии. Созданные ИИ регуляторы справились с этой задачей лучше существующих природных вариантов.
Предложенный метод превосходит другие компьютерные подходы по сочетанию функциональной активности, точной специфичности и сохранению разнообразия генерируемых последовательностей. DNA-Diffusion является эффективным инструментом для создания компактных и высокоспецифичных регуляторных элементов, что важно для развития генной терапии и изучения принципов работы генов.
Технология целенаправленного конструирования регуляторных фрагментов ДНК может лечь в основу создания более точных и безопасных генетических препаратов. Метод позволяет тонко настраивать клеточные функции, что представляет интерес как для фундаментальных исследований, так и для практической медицины.[1]
Успешное применение генной терапии для лечения Синдрома Ушера
29 июля 2025 года итальянские ученые из Университета Кампании имени Луиджи Ванвителли сообщили о разработке революционного метода генной терапии, способного обратить вспять редкое и ранее неизлечимое заболевание сетчатки глаза. Первые данные, опубликованные через год после начала клинического исследования, свидетельствуют о значительном улучшении зрительной функции без каких-либо серьезных побочных эффектов.
Речь идет о лечении Синдрома Ушера — редкого генетического заболевания, которое приводит к врожденной нейросенсорной тугоухости и прогрессирующей потере зрения. Данный недуг (тип 1b) вызван мутациями в гене MYO7A, который слишком велик для переноса стандартными вирусными векторами, обычно используемыми в генной терапии. Решение проблемы предложили специалисты Института генетики и медицины Telethon (TIGEM) в Поццуоли. Исследователи разработали инновационную двухвекторную технологию: два модифицированных вируса доставляют по половине гена каждый, что позволяет клетке собрать информацию и произвести полноценную функциональную версию белка.
Первая процедура с применением данного метода была проведена в офтальмологической клинике Университета Кампании имени Луиджи Ванвителли. Пациентом стал мужчина в возрасте 38 лет. Через год после выполнения терапии он сообщил о значительном улучшении как ближнего, так и дальнего зрения, даже в условиях низкой освещенности.
| | Теперь я могу узнавать лица, видеть на работе проходы на складе и читать субтитры по телевизору. Речь идет не только о том, чтобы лучше видеть, — я начинаю жить заново, — отмечает пациент. | |
В ходе новой генной терапии не зарегистрировано серьезных побочных эффектов, а те, что все же возникали, были легкими, редкими и легко поддающимися лечению.[2]
Мышечную дистрофию начали лечить генной терапией, но она убила троих человек
Управление по контролю качества пищевых продуктов и лекарственных средств США приостановило клинические испытания экспериментальной генной терапии для лечения поясно-конечностной мышечной дистрофии и временно запретило поставки препарата «Элевидис» после регистрации смертей трех пациентов в ходе исследований. Компания Sarepta Therapeutics добровольно остановила все поставки препарата в США для выяснения обстоятельств инцидентов. Об этом стало известно в июле 2025 года. Подробнее здесь
Впервые врожденную слепоту вылечили с помощью генной терапии
Группа врачей из больницы Great Ormond Street в Лондоне успешно применила генную терапию для лечения врожденной слепоты у четырех детей с редким наследственным заболеванием. Результаты первого в мире подобного вмешательства опубликованы в феврале 2025 года. Подробнее здесь.
2024
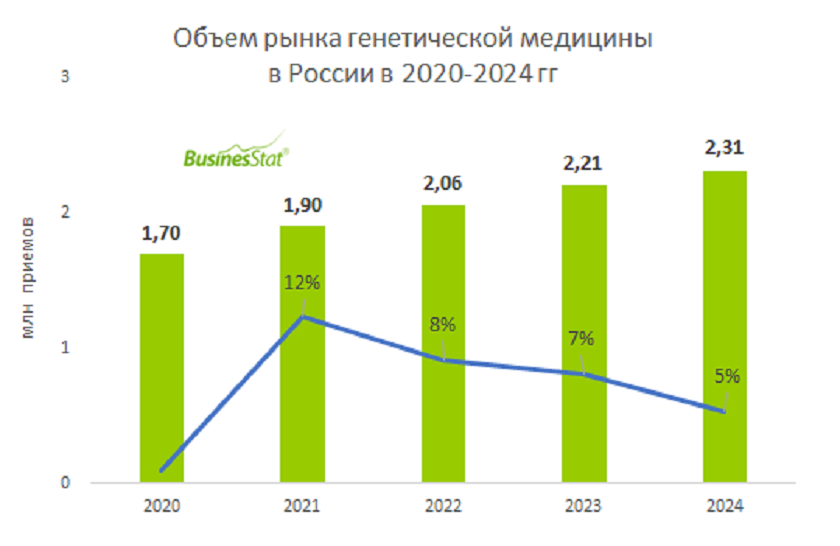
Рост объёма российского рынка генетической медицины на 5% до 2,31 млн приёмов
Объём рынка генетической медицины в России в 2024 году вырос на 5% и достиг 2,31 млн приёмов. Прирост замедлился по сравнению с предыдущими годами, когда темпы роста достигали 12%. Об этом свидетельствуют данные исследования «Анализ рынка генетической медицины в России», опубликованного BusinesStat в декабре 2025 года.
За 2020–2024 годы объём рынка генетической медицины в России вырос на 36%: с 1,7 млн до 2,31 млн приёмов. В 2021 году рынок продемонстрировал максимальный прирост на 12%, объём достиг 1,9 млн приёмов. В 2022 году рост составил 8%, рынок увеличился до 2,06 млн приёмов. В 2023 году темп прироста замедлился до 7%, объём достиг 2,21 млн приёмов.
После пандемии люди стали внимательнее относиться к своему здоровью, что способствовало увеличению востребованности комплексных генетических исследований. Рынок демонстрирует устойчивый рост, хотя темпы прироста постепенно снижаются. Это свидетельствует о переходе от фазы активного освоения рынка к более зрелому этапу развития.
Генетические исследования включают тесты на предрасположенность к различным заболеваниям, на происхождение, для подбора эффективных лекарственных средств, для составления индивидуальных рационов питания, программ тренировок, ухода за кожей и волосами. Расширение спектра доступных исследований привлекает новых клиентов.
Россиянам стали доступны direct-to-consumer ДНК-тесты, которые не требуют посещения лаборатории. Пациент собирает материал, например слюну, в контейнер, передаёт курьеру или отправляет по почте и позднее получает подробные результаты, их расшифровку и консультацию генетика в личном кабинете на сайте или в приложении.
Такой опыт сделал генетические исследования доступнее и вызвал интерес к ним у россиян. Упрощение процедуры прохождения тестирования снизило барьеры для входа на рынок. Клиенты получили возможность проходить исследования без необходимости посещения медицинских учреждений, что особенно важно для жителей отдалённых регионов.
Ведущими специализированными генетическими лабораториями в России являются:
- ООО «Геномед»;
- ООО «Эвоген»;
- ООО «Генотек»;
- ООО «Медикал Геномикс»;
- ПАО «ЦГРМ «Генетико».[3]
Расходы на клеточную и генную терапию в мире за год достигли $10,75 млрд
В 2024 году объем глобального рынка клеточной и генной терапии достиг $10,75 млрд. Более половины от общемировых затрат пришлось на североамериканский регион. Об этом говорится в обзоре Grand View Research, с которым Zdrav.Expert ознакомился в конце июля 2025 года.
Клеточная терапия — быстро развивающееся направление медицины. Технология предполагает перенос в организм пациента новых или модифицированных в лабораторных условиях клеток для восстановления органов и тканей, поврежденных в результате травмы или заболевания. Клеточная терапия может использоваться при лечении широкого спектра недугов, в число которых входят иммунодефицитные состояния, патологии сердечнососудистой системы, атеросклероз конечностей и сосудов головного мозга, Болезнь Альцгеймера и Болезнь Паркинсона, аутизм, патологии почек, хронические заболевания желудочно-кишечного тракта и др. В частности, набирает обороты CAR-T-клеточная терапия: это форма иммунотерапии, которая использует иммунные клетки пациента для целенаправленного уничтожения злокачественных образований.
В свою очередь, генная терапия предусматривает введение, изменение или удаление генетического материала с целью лечения или профилактики заболеваний. Метод может применяться при терапии наследственных, мультифакториальных и ненаследственных (инфекционных, злокачественных и др.) недугов. В отличие от многих других технологий, генная терапия может обеспечить длительный или даже постоянный эффект, поскольку направлена на коррекцию на уровне ДНК. Кроме того, обеспечивается персонализированный подход к лечению с учетом индивидуальных особенностей конкретного пациента.
Одним из основных драйверов рынка авторы исследования называют технологические достижения, в частности, в области редактирования генов (CRISPR-Cas9). Инструменты нового поколения обеспечивают точную коррекцию генов с минимизацией нежелательных эффектов. Расширению отрасли способствуют стратегические партнерства между биотехнологическими компаниями, крупными фармацевтическими корпорациями и исследовательскими центрами. Ведущие игроки вкладывают значительные средства в развитие технологий клеточной и генной терапии.
Вместе с тем существуют и сдерживающие факторы. Исследования и разработки в рассматриваемых сферах требуют больших временных затрат и огромных финансовых вложений. Существуют этические вопросы, связанные в том числе с внесением изменений в гены человека. Кроме того, возможны побочные эффекты.
Авторы исследования выделяют такие рыночные сегменты, как онкология, кардиология, центральная нервная система, опорно-двигательный аппарат, инфекционные заболевания, дерматология, эндокринная система, иммунология, офтальмология, гематология, гастроэнтерология и пр. В 2024 году около половины расходов пришлось на первое из перечисленных направлений. В географическом плане доминирует Северная Америка с долей 50,9%, или примерно $5,47 млрд. Это обусловлено развитой инфраструктурой клинических исследований в регионе, высокой концентрацией биотехнологических и фармацевтических компаний, а также регуляторной поддержкой инновационных методов лечения. В глобальном масштабе значимыми игроками названы:
- Iqvia;
- Icon;
- LabCorp;
- Charles River Laboratories;
- Parexel International;
- Syneos Health;
- Medpace;
- Thermo Fisher Scientific;
- Novotech;
- Veristat.
Аналитики Grand View Research полагают, что в дальнейшем среднегодовой темп роста в сложных процентах (CAGR) составит 15,58%. Таким образом, к 2033 году расходы могут увеличиться до $39,41 млрд.[4]
Разработанная американской Bluebird bio генная терапия от болезней нервной системы привела к семи случаям рака крови
В середине октября 2024 года стало известно, что в ходе исследований генной терапии Skysona производства компании Bluebird bio были обнаружены семь случаев рака крови. Подробнее здесь
Глаукому начали лечить генной терапией
В середине сентября 2024 года ученые из Тринити-колледжа в Дублине представили многообещающую генную терапию для лечения глаукомы. Ранее та же команда открыла возможность генной терапии сухой формы возрастной макулярной дегенерации, другого заболевания глаз, ведущего к слепоте. Подробнее здесь
Разработан революционный метод генной терапии, который улучшил зрение пациентов в 10 000 раз
В середине сентября 2024 года были опубликованы результаты испытания новой генной терапии врожденного амавроза Лебера, который позволяет улучшить зрение пациентов в 100 и даже 10 000 раз.
Врожденный амавроз Лебера 1 типа (LCA1) — это редкое наследственное заболевание сетчатки, которое развивается вследствие мутаций в гене GUCY2D и приводит к почти полной потере зрения начиная с младенческого возраста. Новая генная терапия ATSN-101 воздействует непосредственно на причину заболевания, то есть на дефектный ген GUCY2D: при этом виде лечения функциональная копия этого гена доставляется непосредственно в фоторецепторные клетки сетчатки, тем самым восстанавливая их функциональность и позволяя коре головного мозга получать и анализировать данные об окружении. Исследование, опубликованное в журнале Lancet, включало 15 пациентов с этим заболеванием, которым вводили препарат однократно в один глаз, а затем сравнивали улучшение по сравнению с другим глазом. У всех пациентов отмечался качественный скачок.
Улучшение зрения в 10 000 раз равносильно тому, что «пациент теперь может видеть свое окружение в лунную ночь на улице, хотя до начала лечения ему требовалось яркое освещение в помещении для того, чтоб что-то увидеть», как отметил ведущий автор исследования Артур Сидесиян, директор Центра наследственных дегенераций сетчатки.
Важно отметить, что наблюдаемое улучшение зрения оказалось достаточно стойким – улучшение было зарегистрировано уже на 28-й день исследования и сохранялось до 12-го месяца. По словам исследователей, один из пациентов даже смог передвигаться на улице в полночь, используя только костер в качестве источника света. Ученые надеются, что этот революционный препарат сможет стать настоящей панацеей для пациентов с врожденным амаврозом Лебера.[5]
Новая революционная генная терапия успешно восстановила слух у глухого малыша
9 мая 2024 года британские исследователи из больницы Адденбрука в Кембридже сообщили об успешном использовании революционной генной терапии, которая позволила восстановить слух у глухого малыша. Это событие, по заявлениям медиков, знаменует собой новую эру в лечении глухоты.
Пациентом стала Опал Сэнди (Opal Sandy), которая родилась со слуховой невропатией. Это патологическое состояние, при котором нарушается проведение нервного импульса от внутреннего уха в головной мозг. В норме данную функцию выполняет слуховой нерв, однако при его поражении передача сигналов нарушается.
Слуховая нейропатия может быть вызвана дефектом гена OTOF, который производит белок под названием отоферлин. Это позволяет клеткам уха взаимодействовать со слуховым нервом. Новая терапия, разработанная биотехнологической фирмой Regeneron, предусматривает «отправку» рабочей копии гена в ухо для устранения проблемы с передачей сигналов.
Через четыре недели после проведения генной терапии в правое ухо Опал Сэнди начала реагировать на звуки, даже когда специальный имплантат в левом ухе был отключен. Клиницисты отметили стабильное улучшение слуха у девочки, которой по состоянию на май 2024 года исполнилось 18 месяцев. Более того, уровень слуха тихих звуков, таких как шепот, приблизился к нормальному. Малышка может реагировать на голоса своих родителей и произносить простые слова.
Генная терапия специально предназначена для детей с мутациями OTOF. Для переноса рабочего гена в организм пациента используется безвредный вирус. Доктор Ричард Браун (Richard Brown), один из участников исследования, говорит, что развитие геномной медицины и альтернативных методов лечения жизненно важно для пациентов во всем мире. Этот подход дает надежду детям с ранее неизлечимыми заболеваниями.[6]
Начали применять новую генную терапию, которая восстанавливает слух у людей с врожденной глухотой
24 января 2024 года Массачусетская офтальмологическая и отоларингологическая больница (MEE) сообщила о том, что американские и китайские специалисты успешно внедрили генную терапию для восстановления слуха у детей, страдающих врожденной глухотой. Речь идет о мутации DFNB9 в гене OTOF (белок отоферлин), которая приводит к невозможности передачи звуковых сигналов от уха к мозгу.
Отмечается, что потеря слуха затрагивает более 1,5 млрд человек во всем мире, причем около 26 млн из них страдают врожденной глухотой. Нарушения слуха у детей более чем в 60% случаев обусловлены генетическими причинами. Например, DFNB9 — это наследственное заболевание, при котором ребенок рождается глухим.
В исследовании приняли участие 6 детей с DFNB9, которые наблюдались в течение 26 недель в больнице Фуданьского университета в Шанхае. У всех пациентов, возраст которых составлял от 1 до 6 лет, были две мутантные копии гена OTOF, и до лечения у них наблюдалась полная потеря слуха. Генная терапия, которую они получили, содержала аденоассоциированные вирусы, чьи гены были удалены и заменены геном OTOF. Терапия выполнялась через мембрану, отделяющую среднее ухо от внутреннего.
Сообщается, что у всех детей, кроме одного, отмечено стабильное восстановление слуха в течение 26 недель после выполнения процедуры. Улучшения начали проявляться примерно через четыре–шесть недель после лечения, наряду с улучшением восприятия речи. По заявлениям специалистов, лечение не вызвало каких-либо серьезных побочных эффектов, хотя наблюдались лихорадка и изменения в количестве лейкоцитов. В целом, как отмечается, исследование подтверждает безопасность и эффективность генной терапии при лечении DFNB9, а также говорит о возможности применения метода при других формах генетической потери слуха.[7]
2023: Хроническую боль начали лечить генной терапией
27 июля 2023 года американские исследователи из Нью-Йоркского университета сообщили о разработке новой методики лечения хронической боли на основе генной терапии. Подробнее здесь.
См. также
- Генетическая инженерия (генная инженерия)
- Национальная база генетической информации
- Геном
- Генетические банки данных (биобанки, биорепозитории, хранящие биологические образцы)
- Геномика и биоинформатика в России
- Хромосомы
Примечания
- ↑ Generative AI creates synthetic regulatory DNA sequences for precision gene control
- ↑ Usher Syndrome: Promising Early Results from a New Gene Therapy Developed at TIGEM
- ↑ За 2020-2024 гг объем рынка генетической медицины в России вырос на 36%: с 1,7 до 2,3 млн приемов.
- ↑ Cell And Gene Therapy Clinical Trials Market Size,Share & Trends Analysis Report
- ↑ Gene therapy yields 100x vision average improvement, with a few reaching 10,000x
- ↑ Baby born deaf can hear after breakthrough gene therapy
- ↑ Gene Therapy Restores Hearing in Children with Hereditary Deafness